PROTOTIPO DE DISPOSITIVO MÉDICO DE APOYO AL DIAGNÓSTICO DE CANCER DE PRÓSTATA MEDIANTE TEORÍAS DE CLASIFICACIÓN DE IMAGEN CON DEEP-LEARNING
Los algoritmos de Deep-Learning, y en concreto las Redes Neuronales por Convoluciones (CNNs), se han convertido rápidamente en la metodología más atractiva para el análisis de imágenes en diferentes campos, y en particular en el ámbito médico. En la literatura se pueden encontrar múltiples trabajos a este respecto, tal como se repasa en los antecedentes; en clasificación de imágenes, detección de objetos, segmentación y otras tareas. Existen áreas médicas donde se ha profundizado más, como en la neuronal, retinal, pulmonar, patología digital, cardíaca, abdominal o músculo-esqueleto, entre otras. Las CNNs consisten en una serie de capas de filtrado por convoluciones de una imagen de entrada. En cada capa se realizan múltiples convoluciones con diferentes filtros con el objetivo de extraer determinadas características de la imagen. En la primera capa se extraen características más simples, como orientaciones, detecciones de bordes, etc. En las siguientes capas se realizan otro tipo de filtros que permiten la combinación de las características extraídas de capas anteriores para detectar morfologías o distribuciones particulares en la imagen. Tras una serie de capas de convolución se utiliza un clasificador neuronal para ofrecer una clase de salida con una probabilidad de éxito asociado a la decisión. Estas CNNs requieren que los filtros estén programados de forma adecuada para obtener la clasificación esperada. La obtención de estos filtros se realiza mediante un proceso de entrenamiento. Uno de estos mecanismos es el denominado Back-Propagation, el cual mediante iteraciones sobre una base de datos permite indicar a la red neuronal, para una imagen de entrada, cuál debe ser su clasificación y de esta forma el algoritmo Back-Propagation realiza un ajuste de los valores de todos los filtros de las capas de convolución para poder ofrecer la misma salida de clasificación con una imagen de entrada similar. En grandes rasgos, cuantas más imágenes se tengan para entrenar, más precisión se obtendrá de la CNN en la clasificación.
La gran ventaja de aplicar este tipo de técnicas al diagnóstico por imagen es que, al ser sistemas de aprendizaje automático capaces de ajustarse a las características significativas que tienen las imágenes en común, no requieren del uso de sofisticadas técnicas estadísticas, o de otro tipo, que puedan emular el conocimiento que un erudito en la materia tiene sobre el tipo de imagen y diagnóstico que se está buscando, sin ser dependientes de condiciones de iluminación, orientaciones, etc. Mediante el uso de una correcta base de datos con el número suficiente de casos y variedad de los mismos, se puede entrenar un sistema de deep-learning, para que ofrezca un pre-diagnóstico, más la probabilidad de error de este prediagnóstico.
El equipo proponente de este proyecto cuenta con experiencia previa en el desarrollo de sistemas CNNs para clasificación de imagen tanto para aplicaciones médicas como de ingeniería [1] . Gracias a las colaboraciones con el grupo VITRO S.A. se han comenzado a desarrollar las arquitecturas de CNNs más adecuadas para el diagnóstico por imagen en instrumentos robotizados de técnicas de hibridación de ADN para diagnóstico de infecciones por virus del tipo HPV, Zoonosis, Sepsis, etc. [2]
PROMETEO se pretende validar el uso de esta teoría a la ayuda al diagnóstico de cáncer mediante el análisis de imagen. Como demostración de la eficacia del “Deep-learning”, en este proyecto nos vamos a centrar en el cáncer de próstata y el análisis de imagen será a partir de biopsia de tejido prostático obtenido por fusión de la punción con guiado radiológico. Generalmente, una vez realizada la biopsia, el patólogo analizará la estructura celular del tejido en un plazo de entre 1 y 7 días, dependiendo varios factores. Con la solución que se plantea se pretende reducir considerablemente el tiempo de diagnóstico. Una vez validada esta técnica de “Deep-learning”, la cual podrá ser extendida a la ayuda al diagnóstico de otros tipos de cáncer, es objeto del proyecto diseñar un equipo informático, dotado de los aceleradores hardware necesarios, para que el diagnóstico pueda obtenerse en tiempo real (o con el retraso mínimo) para el patólogo. Se pretende, igualmente, dar los pasos necesarios para la comercialización del equipo a través de la empresa de base tecnológica, y Spin Off de la Universidad de Sevilla, creada en 2014, denominada COBER S.L.
El proyecto se divide de las siguientes fases:
1. Obtención de la base de datos de entrenamiento. El equipo está actualmente en contacto con patólogos de hospitales nacionales especializados en cáncer de próstatas para la creación una base de datos para el entrenamiento de una CNN. Se está realizando una aplicación software, para ser usada por los patólogos, para que puedan localizar y marcar fácilmente las zonas de tejido que muestran signos de cáncer, así como el tipo de cáncer que se presenta en el tejido, siguiendo la escala de Gleason. Guardando las coordenadas marcadas por el patólogo, la tipología detectada, así como una referencia al archivo de imagen original; se puede automatizar la creación de la base de datos de entrenamiento.
2. Diseño y validación de la CNN para detección de cáncer de próstata. Existen múltiples arquitecturas de CNN en la bibliografía, las cuales se diseñan mediante técnicas de prueba y error, para ajustarse al problema planteado con el mínimo número de recursos computacionales. Es decir, no existe hasta la fecha una receta para el diseño de una CNN que se ajuste al problema a resolver minimizando los recursos. En esta fase se diseñará una CNN de tamaño adecuado a nuestro problema, tomando de referencia trabajos previos similares, y se entrenarán con la base de datos de la fase anterior. Posteriormente se validará la CNN. Para ello se harán uso de las herramientas software disponibles como Caffe o Theano.
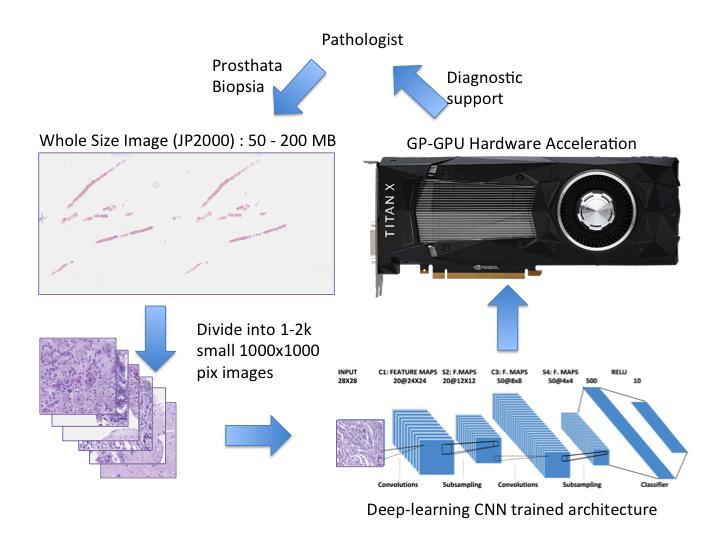
3. Desarrollo de equipo informático para ejecución de la CNN sobre Whole Size Images de próstatas en tiempo real o con latencias reducidas. Una vez se tenga el algoritmo CNN diseñado y validado se diseñará un equipo informático tipo “barebone”, dotado de una o varias tarjetas tipo GPU para aceleración de la ejecución de la CNN ya entrenada. Se desarrollará, igualmente, una interfaz de usuario software amigable para su uso en entornos sanitarios. La figura 1 muestra un diagrama del ciclo de ejecución del sistema informático desde la obtención de la imagen JP2000 hasta la obtención del resultado de ayuda al diagnóstico. La imagen capturada de resoluciones 100Kx200K píxeles se divide en subimágenes de menor resolución (1024×1024 píxeles) y que contengan tejido, y se procesan en el acelerador HW (basado en GP-GPU o FPGA) de acuerdo con la CNN de arquitectura elegida y debidamente entrenada. El resultado en forma de probabilidad se usará para graduar un mapa de colores de verde a rojo sobre la imagen inicial para indicar al patólogo las zonas con sospecha detectadas.
4. Fase de pruebas y validación en hospitales. El sistema diseñado se llevará e instalará en varios hospitales para ser testados por los patólogos y extraer estadísticas de tasas de éxito del sistema y de grado de satisfacción del personal sanitario.
5. Campaña de presentación, divulgación y marketing del producto en hospitales públicos y privados, así como en ferias y congresos médicos, para comercialización del sistema.
[1] Alessandro Aimar, Hesham Mostafa, Enrico Calabrese, Antonio Rios-Navarro, Ricardo TapiadorMorales, Iulia-Alexandra Lungu, Moritz B. Milde, Federico Corradi, Alejandro LinaresBarranco, Shih-Chii Liu, Tobi Delbruck. “NullHop: A Flexible Convolutional Neural Network Accelerator Based on Sparse Representations of Feature Maps”. arXiv:1706.01406v1
[2] Juan P. Dominguez-Morales, A. Jimenez-Fernandez, S. Vicente-Diaz, A. Linares-Barranco; A. Olmo-Sevilla, and A. Fernandez-Enriquez. “A Protocol Generator Tool for Automatic in-vitro HPV Robotic Analysis”. Springer. ROBOT-2017.
Empresas colaboradoras:
COBER SL (http://www.t-cober.es/)
Grupo Vitro (http://www.vitro.bio/)
IP: Alejandro Linares Barranco
Programa: PAIDI-2020. Transferencia
Funding by: Conserjería de Economía, Conocimiento, Empresas y Universidad
Start date: 01-02-2020
End date: 31-01-2021
Researchers:
- Claudio Amaya Rodríguez
- Elena Cerezuela Escudero
- Antón Civit Balcells
- Lourdes Durán López
- Juan Pedro Domínguez Morales
- Manuel Jesús Domínguez Morales
- Angel Jiménez Fernández
- Gabriel Jiménez Moreno
- Francisco Luna Perejón
- Rafael Paz Vicente
- Antonio Ríos Navarro
- Saturnino Vicente Díaz

